不信人言:Nectome 大腦保存技術的第三方證據
我們展示了來自大腦保存基金會與生存與繁榮基金會的獨立驗證結果,證明 Nectome 的醛類穩定低溫保存法能在理想與現實條件下,完整保留大腦的奈米級結構以供未來復原之用。
大腦保存基金會(Brain Preservation Foundation)與生存與繁榮基金(Survival and Flourishing Fund)的獨立驗證——目前的結果
建立獨立驗證機制
非凡的主張需要非凡的證據。在我之前的文章「減少死亡」中,我提到我的公司 Nectome 已經:
創造了一種用於未來復活目的的全身體、全大腦人類臨終保存新方法。我們的方案能夠保存體內的每一個突觸和每一個細胞,其細節足以滿足當前神經科學所認為的長期記憶保存標準。它與室溫下的傳統葬禮相容,且在低溫下可穩定保存數百年。
在這篇文章中,我們將深入探討這些主張的證據,以及 Nectome 建立嚴謹、獨立驗證方法的整體方針——這是我希望參與的保存事業之基石。
要達到目前的技術水準,需要跨越兩個主要的發展里程碑:
-
理想化保存:一種能夠在理想實驗室條件下保存小型和大型動物大腦奈米結構的方法。具體來說,如果允許我們完美控制死亡的時間和條件,我們能否良好地保存動物?
這項工作(2015-2018 年)催生了一項全新技術——醛類穩定冷凍保存(Aldehyde-Stabilized Cryopreservation, ASC)。這項技術經過大腦保存基金會(BPF)的 Ken Hayworth 為期三天的馬拉松式審查,期間我在他的監督下保存了一隻兔子和一隻豬。隨後,他利用電子顯微鏡檢查了這兩個大腦的多個樣本。我在《冷凍生物學》(Cryobiology)雜誌上發表了 《醛類穩定冷凍保存》 論文,並因此獲得了 BPF 頒發的小型和大型哺乳動物獎項。透過這項工作,我們獲得了存在性證明:在奈米級細節上長期保存整個大腦是絕對可以實現的,至少在實驗室條件下是如此。 -
現實世界保存:一種能夠在現實條件下保存大腦奈米結構的方法。具體來說,我們能否將實驗室方法擴展到受限於現實世界人類案例的法律要求和實務限制下?
將該技術調整以適應混亂的現實條件(2018-2025 年)花費了更多的開發時間,產生了許多關於人類保存可行與不可行性的見解,並塑造了我們未來的整體保存方針。在一個令人難忘的案例中,當我們終於擁有一項符合我們嚴謹標準的豬隻保存技術時,我們再次進行了馬拉松式的現場演示。 生存與繁榮基金(SFF) 的聯合創始人 Andrew Critch 親自見證了在模擬人類保存條件下對大鼠進行的保存;所得的大腦樣本在諮詢加州大學柏克萊分校顯微鏡實驗室和芝加哥大學 Kasthuri 教授後進行了成像。基於這次演示,Andrew 推薦我們獲得投資,我們隨後也收到了這筆資金。這項現實世界技術已作為預印本提交:《與人類醫師輔助死亡方案相容的大型哺乳動物全腦超微結構保存》。
本文的其餘部分將致力於解析這些結果。
在開始之前有五點簡短說明:
- 應 大眾要求,本文專門討論奈米結構的保存品質——即在整個大腦和身體中實現詳細的保存水平,使突觸可以追溯到其來源神經元,並保留亞突觸細節,其效果與神經科學研究中使用的傳統固定方法一樣好。關於「全身體奈米級保存足以實現未來復活」的論點,我將推遲討論,因為它值得專門寫一篇文章。
- 本文的草案已由大腦保存基金會主席 Ken Hayworth 審閱,他簽署確認其為:「對大腦保存基金會、其歷史、Ken 的個人動機以及 BPF 兩項保存獎結果的準確描述」。自那以後,我沒有對內容進行實質性修改。
- 本文的草案已由生存與繁榮基金聯合創始人 Andrew Critch 審閱,他簽署確認其為:「對他訪問 Nectome 評估其保存技術以及隨後結果的準確描述」。同樣,自那以後未經實質修改。
- 利益衝突說明:在研究所期間,我曾在大腦保存基金會擔任約一年的志工。在深入了解大腦保存後,我決定辭去志工身份並在 Ken 的批准下親自參賽。
- 您可能會注意到,我在本文中引用的一些參考資料將我的工作歸功於我的舊名 Robert McIntyre。現在我使用我的選定名 Aurelia Song。
在實驗室中:Ken Hayworth 與 BPF
什麼是大腦保存基金會?
Ken Hayworth 是一位神經科學家,目前任職於 Janelia 研究園區(隸屬於霍華德·休斯醫學研究所 HHMI)。2010 年,Ken 創立了 大腦保存基金會(BPF) 並發起了「大腦保存獎」,以此向神經科學和人體冷凍保存社群發起挑戰。他希望看到研究人員提供證據,證明其保存技術符合神經科學的合理標準。
作為一名連接組學家(connectomicist),Ken 習慣於觀察使用電子顯微鏡創建的大腦組織 3D 模型。這些模型是從使用神經科學領域多年來標準的高品質固定法保存的大腦中掃描出來的。在對神經科學進行了深入思考後,Ken 得出結論:這種水平的物理保存極有可能捕捉到未來修復一個人所需的資訊,我也傾向於同意這一點。同樣,我將在未來的文章中討論這個問題。
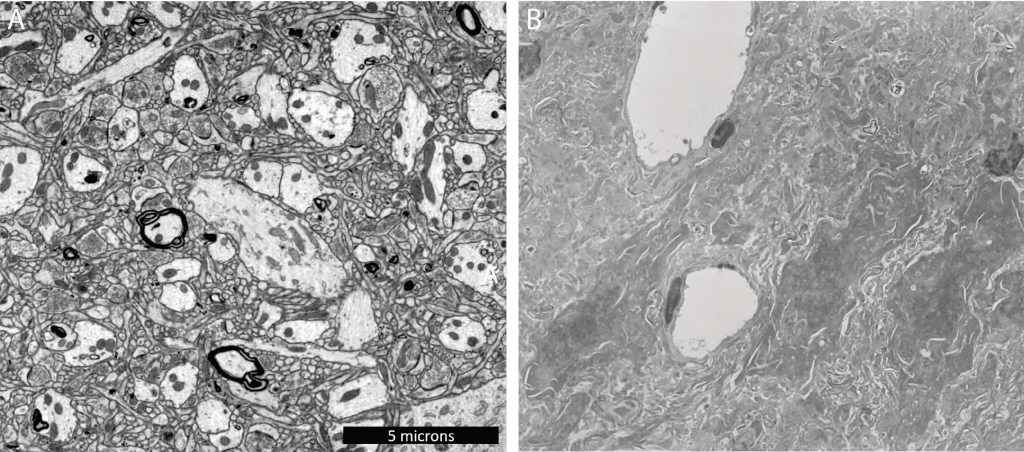
但來自人體冷凍保存社群的電子顯微照片與他在實驗室通常看到的並不一樣。那裡沒有 3D 分析,只有單幀圖像。更糟糕的是,組織嚴重脫水,導致難以或無法判斷組織是否具有 可追溯性(traceable),也就是說,每個突觸是否都能追溯回其來源神經元。
上方的圖像是取自 BPF 的 認證(Accreditation) 頁面。左圖是「典型」大腦組織的樣子——即 Ken 和其他神經科學家習慣研究的那種。右圖是經過冷凍保護的動物大腦^([1])。它看起來更像「漩渦狀」,因為它被冷凍保護劑脫水了。Ken 發起大腦保存獎的部分原因,就是挑戰冷凍保存社群產生更像左圖的影像,以便他們能更好地評估其保存技術是否有效。
對 Ken 和我來說,這是一個巨大的問題。有很多方法會導致大腦變得無法追溯,而能保存其結構的方法相對較少。在沒有相反證據的情況下,我們必須預設大腦是不可追溯的。這反過來又讓人質疑大腦中保存的資訊是否充足。
除了挑戰冷凍保存社群外,Ken 還希望向神經科學界發起挑戰。他希望神經科學家能利用他們先進的組織準備和分析方案,設計出一種能保存人類以供未來復活的技術。
Ken 受到成功的 Ansari X Prize 啟發,決定以獎金的形式發布挑戰。他從一位秘密捐贈者那裡籌集了 10 萬美元^([2]),並制定了 競賽規則:大腦必須以具備連接組可追溯性的方式保存,且保存狀態必須極可能維持至少 100 年。針對「小型」哺乳動物大腦(如兔子、小鼠或大鼠)設有小型獎項,而「大型」哺乳動物大腦(豬、羊等)則可贏得全部獎項。
我無法言喻大腦保存獎對於推動保存研究領域的影響有多大。那 10 萬美元激勵我建立了我的方案,並引導了數百萬美元的投資進入更好的保存技術。我希望能看到更多科學獎項;我認為它們能幫助研究室的年輕人,讓他們有理由將資源投入到他們熱衷的重要項目中。像 2014 年的我這樣的年輕研究員,可以去跟上司說:「這不只是個人項目,這是為了這個獎項。」
在理想條件下有效的方案:醛類穩定冷凍保存(ASC),2015 年
當我開始認真研究保存技術時,我發現人體冷凍保存和神經科學面臨著相反的問題。神經科學家幾乎可以立即使用醛類^([3])保存大腦,但沒有長期策略來讓大腦在一百年或更長時間內保持完好。與此同時,冷凍保存者在向大腦灌注冷凍保護劑時難以避免損傷,但他們知道如何將灌注後的大腦冷卻到玻璃化溫度並無限期保存。
顯而易見的解決方案是結合這兩種方法。我可以利用固定技術卓越的生物組織穩定能力,爭取時間將冷凍保護劑緩慢地引入大腦,以避免快速脫水造成的毀滅性損傷。然後,就可以安全地將大腦玻璃化以進行長期保存。
我花了九個月的時間才理清所有細節。最困難的部分是弄清楚如何讓冷凍保護劑穿過血腦屏障:事實證明,即使是非常長的灌注時間,本身也不足以防止脫水。不過,最終我成功在兔子(我當時使用的小型哺乳動物模型)上實現了這項技術。將該方案修改以適用於豬隻只花了我一天的時間,而且第一次嘗試就成功了。我在《冷凍生物學》(Cryobiology)上發表了這項研究結果:《醛類穩定冷凍保存》,這是贏得大腦保存獎的第一步。
大腦保存基金會的獨立驗證
獲獎的下一步需要 BPF 的直接驗證。如果您有興趣,可以在 這裡 閱讀他們的完整方法論。
當時,我在 21st Century Medicine 工作。Ken Hayworth 飛到我的所在地,加入了我為期三天、從黎明到黑夜的馬拉松式工作。期間我保存、玻璃化、復溫並處理了一隻兔子和一隻豬。每當 Ken 沒有親自觀察大腦樣本時,他都會用防篡改貼紙將其封存,以確保監管鏈完整。當我完成電子顯微鏡樣本的準備後,Ken 親自在 Janelia 進行了樣本的切片和成像。
這是我以前從未見過的嚴謹程度,肯定遠遠超出了《冷凍生物學》論文的同行評審。這是我欽佩 Ken 的地方,我也對此深表感激。保存是一件值得嚴謹對待的事情!
BPF 使用高解析度聚焦離子束切削和掃描電子顯微鏡(FIB-SEM)準備影像。這項技術可產生高達 4 奈米的解析度;Ken 以 8 奈米和 16 奈米的各向同性解析度掃描了參賽作品。結合影像的 3D 特性,這足以檢查大腦樣本並確定突觸(通常約 100 奈米寬)是否可追溯。
當然,對整個大腦進行成像遠遠超出了我們目前的能力。Ken 透過分析從大腦不同區域隨機選取的多個樣本來彌補這一點。BPF 發布了所有影像和原始 3D 數據文件,至今仍可查閱。我在下方附上了豬腦的影像——點擊影像可觀看顯示完整 3D 成像的 YouTube 影片。每個樣本都來自經過保存、玻璃化和復溫的大腦。
Ken Hayworth 與普林斯頓/麻省理工學院的神經科學家 Sebastian Seung 共同擔任 BPF 的評審團成員。Sebastian 是《我是我的連接組》(I am my Connectome)一書的作者,也是 FlyWire 項目的主要貢獻者。他們一起審查了 3D 影像,判斷其品質,並在影像堆疊中追蹤神經元。最終,他們一致同意我贏得了獎項。
相關連結:
我以此作為證據,證明將大型哺乳動物大腦保存在可追溯狀態、保留每個突觸、並使其穩定維持一百年以上(關於「一百年」的部分,我們將在未來關於保存熱力學的文章中討論)是可能的。^([4])
但 ASC 並非故事的全貌,因為它必須在 死前 進行。世界各地的臨終法律並非為保存末期病患而設計,也不允許將 ASC 作為一種選擇。為了創造出可行的方案,我要麼必須找到一種在 死後 進行保存的方法,要麼努力將 ASC 納入臨終法律。我選擇了讓保存技術在死後也能奏效。
在實務現場:Andrew Critch 與 SFF
讓保存技術在現實世界中奏效,在概念上其實很簡單。原始方案需要三項修改才能在死後發揮作用:
- 心臟驟停必須迅速發生,以避免死前的大腦損傷。我們發現這需要「醫療助死」(MAiD)。
- 在心臟驟停前必須使用抗凝血劑。
- 手術必須 快。灌注需要在死亡後不到 12 分鐘內開始。
我父親曾告訴我一個他大學生物教授的故事。開學第一天,教授讓每個人翻開課本,閱讀最後幾章中的第一段。教授隨後告訴大家,他花了 30 年才寫出那一段。我現在更能理解那位教授的感受了。我花了九個月創造了 ASC,卻花了九年時間才將其修改為適應當前法律環境,並寫下上述那三項修改。
我不會在本文中詳述那九年。不過,我想分享一張在這裡首次公開的影像。據我所知,這是世界上保存最完整的人類全腦,它屬於一位死於漸凍症(ALS)並選擇捐獻遺體用於科學研究的 46 歲男性。我在他死後僅 90 分鐘就對他的遺體進行了灌注——這比典型的緊急冷凍保存服務快得多,但仍遠遠超出了 12 分鐘的缺血窗口。
這是我迄今為止完成的最佳人類保存案例的電子顯微照片。來自一例 MAiD 捐贈案例,死後時間約 90 分鐘。中間的大片白色空間是毛細血管。在這裡你可以發現明顯的血管周圍水腫(毛細血管周圍的白色區域),以及令人擔憂的模糊神經氈(neuropil)。我請 Ken Hayworth 審閱了這些影像;他不認為這些影像是可追溯的。此外,這個大腦的某些區域完全未能灌注;這張圖是來自灌注良好的區域。
這是我見過保存最完整的人類全腦。但它也像我保存的其他所有具有明顯死後延遲的人類大腦一樣——不可追溯。這是我(或 BPF)無法接受的品質。看著這種程度的損傷讓我感到恐懼。
我最初以為人類可能有兩小時的死後保存窗口。如果那是真的,我可能會致力於將保存技術整合到全國各地的安寧療護中。但在審查了各種保存條件下的動物和人類電子顯微照片後,很明顯安寧療護模式是行不通的。我們不能等待一個人按照自己的時間表死去然後才開始程序。我們需要他們經歷一個涉及醫療助死(MAiD)的完整過程——而在我們能承諾這種過程的任何益處之前,我們需要在動物身上完善它。
經過大量的改進和專家諮詢,我們最終透過一系列大鼠實驗確定了 12 分鐘的窗口和抗凝血劑的使用。隨後我們簡化了程序,使其能在不到 10 分鐘內在豬屍體上完成,並最終在豬模型中展示了卓越的死後保存效果。我們 最近剛發表了 這些結果:
死後保存的豬腦 3D FIBSEM 影像。我們能夠在 4 分 30 秒內完成手術,遠在關鍵的 12 分鐘窗口內,並獲得了看起來可追溯的結果。更多結果可在 補充材料 中獲得。影片連結如下:
死後保存的豬小腦 H&E 染色光學顯微鏡影像。雖然 FIBSEM 顯示了良好的奈米結構保存,但這張解析度低得多的影像顯示大面積的大腦區域都得到了良好的保存。
摘自 我們的預印本 的圖表。分別為保存不良(左,E)和保存良好(右,F)大腦的 H&E 染色光學顯微鏡影像。請注意左側保存不良組織中存在的明顯白色區域。這是灌注不足和保存受損的有力證據。這兩張影像之間的差異僅在於開始保存的時間延遲了幾分鐘。
SFF 的獨立評估
大約在這個時候,我正在與 Andrew Critch 交談,他是 生存與繁榮基金(SFF) 的聯合創始人。SFF 源於 Jaan Tallinn 的 慈善事業,致力於有感生命的長期生存與繁榮。他們在 2025 年推薦了 3400 萬美元的資助,包括支持 AI Futures Project、Lightcone Infrastructure 和 MIRI 等 眾多項目。
Andrew 有興趣評估 Nectome 以提供 SFF 資助。我們討論後商定了一項具有實質意義的第三方評估:他將前往我們位於華盛頓州溫哥華的實驗室,親自見證並評估一次保存過程,然後親自將樣本帶到電子顯微鏡實驗室進行掃描,最後請他選擇的神經科學家審查樣本品質。如果他滿意所見,他將支持我們向 SFF 資助團隊提出的申請。如果我們沒有達到承諾的品質,他會相應地告知團隊。(SFF 使用分散式資助流程,每位團隊成員都有獨立預算,可根據實質裁量權提出資助建議。)
當 Andrew 到達我們的實驗室時,我們向他介紹了我們的實驗大鼠^([5]),他觀察了我為實驗大鼠注射肝素(我們選用的抗凝血劑),隨後立即進行模擬醫療助死。接著他為我們計時,我在大鼠心臟停止後等待了五分鐘,模擬我在豬或人身上進行手術所需的時間。^([6])
從那時起,我們開始了長達 9 小時的繁瑣過程:血液沖洗、固定以及緩慢提升冷凍保護劑濃度。Andrew 從頭到尾都在觀察。直到深夜保存才完成,Andrew 看著我們取出大鼠大腦並進行目視檢查,確認是否有嚴重的灌注失敗。結果沒有。
此時我們本可以簡單地將大腦放入冷藏庫,然後移交組織進行進一步評估,但我想要展示我們目前的方法有多麼強大。我將大腦切成兩個半球,一個放入 -32°C (-26°F) 的冷藏庫,以展示冷凍保護劑防止冰晶形成的有效性;另一個半球則放入 60°C (140°F) 的實驗室烘箱中過夜。正如冷藏會減緩化學過程,加熱會加速化學過程;在 60°C 下放置 12 小時,保守估計相當於在室溫下放置一週。
第二天我們回來時,我們將每個半球切成紙一樣薄的薄片,Andrew 啟動了他的量子隨機數產生器。^([7]) 他用它從每個半球中隨機選取四片進行分析。我們讓他帶著介紹信前往柏克萊大學的電子顯微鏡核心設施,那裡立即開始了為期一週的組織準備工作,包括染色、樹脂包埋以及切成 90 奈米的切片。
在檢查了電子顯微照片並諮詢了幾位神經科學家後,Andrew 判定我們的保存效果極佳,大腦在連接組學上是可追溯的,且「冷」和「熱」切片的保存品質幾乎完全相同。他推薦我們獲得 55 萬美元的投資,我們隨後也收到了這筆資金。
我們也想向各位展示這些數據。從柏克萊獲得的整體數據集非常龐大;我們樣本中的單張影像約為 5 GB,需要特殊軟體才能查看。我使用 deepzoom 準備了兩張具代表性的影像,如下:
使用 Nectome 方法保存的大鼠大腦樣本,隨後在 60°C 下儲存 12 小時(「熱」儲存)。電子顯微鏡檢查由 柏克萊 EM 核心設施 執行。點擊 這裡 查看完整數據集。
使用 Nectome 方法保存的大鼠大腦樣本,隨後在 -32°C 下儲存 12 小時(「冷」儲存)。電子顯微鏡檢查由 柏克萊 EM 核心設施 執行。點擊 這裡 查看完整數據集。
下一步是什麼?
我們將再次在評論區停留幾個小時,準備回答您的問題。我們的 預售 仍在進行中。下一篇文章將應大眾要求,討論我們如何在實際修復某人之前,判斷保存是否做得足夠好。我們評論區見!
來自我們大鼠大腦演示的單個突觸,在缺血 5 分鐘後保存,並在 60°C 下儲存 12 小時。深色曲線是兩個神經元之間的接合處。突觸底部那些微小的顆粒是單個囊泡,仍然充滿了神經傳導物質,被固定技術懸浮在原位。囊泡附近的較大灰色球體是幫助為突觸供能的線粒體。你可以看到單個細胞骨架的細節。單個蛋白質也仍然存在,儘管在這種解析度水平下無法區分。這就是我所說的「亞突觸」保存。
上一篇:減少死亡
- ^(^) Greg Fahy 最近發布了一份 預印本,討論了冷凍保護劑脫水以及在兔腦中逆轉脫水的一些方法,也請去看看!
- ^(^) 該捐贈者後來被揭露為 Saar Wilf。
- ^(^) 常見的選擇是甲醛或戊二醛。
- ^(^) ASC 實際上比保存每個突觸做得更好——它還保留了幾乎所有的蛋白質、核酸和脂質。我將在以後的文章中詳細介紹相關證據。
- ^(^) 我們給這隻大鼠取名叫 Chandra。Andrew 對我們在動物身上做實驗感到難過,並詢問我們未來是否會嘗試幫助保存和復原非人類動物,我們當然回答了「是」!
- ^(^) 我實際上在豬身上記錄到的時間是 4 分 30 秒。但我喜歡給自己留一點餘地。
- ^(^) 我從未見過其他經常使用量子隨機數產生器(QRNG)來做決定的人 🙂